Alvogenとビジネスパートナーがジェネリックのウリプリスタール5mgの欧州初の認可取得
AsiaNet 78224 (0598)
【パインブルック(米ニュージャージー州)2019年4月9日PR Newswire=共同通信JBN】
Alvogenは9日、ウリプリスタール(Ulipristal)錠に対する16の同時登録手続きを無事終了したと発表した。Alvogenとそのビジネスパートナーは、欧州の複数の国で自社製品の規制認可を受けた。Alvogenは、そのビジネスパートナーと共に、欧州で初の認可取得企業となった。ウリプリスタール5 mg錠に対する科学的承認が得られた。
Alvogenの製品は、Esmya(R)錠のジェネリックで生物学的に同等なバージョンであり、Alvogenの子会社であるLotus Pharmaceuticalsによって完全に自社開発された。Alvogenとそのビジネスパートナーは16の分散手続きを踏み、欧州の16カ国での販売認可を申請していた。Esmya(R)は子宮筋腫の治療に適応される薬である。この製品はAlvogen傘下のLotus Pharmaceuticalsが開発し、世界中の複数の有力ビジネスパートナーにライセンス供与されている包括的ポートフォリオの一部である。
Alvogenのファイサル・カルムア・グローバルポートフォリオ担当副社長は「われわれは、ジェネリックのウリプリスタール錠の認可を喜んでおり、ビジネスパートナーと共に欧州でこの重要な製品の商品化をリードするのを楽しみにしている。Alvogenは、口腔がんポートフォリオ、ホルモン、ソフトジェル、および付加価値ジェネリックを含む複雑なジェネリック医薬品の技術プラットフォーム全体にわたり、社内ジェネリックプロジェクトと規制認可申請待ちの有望なパイプラインを有している」と語った。
▽Alvogenについて
Alvogenは、世界中の患者向けにジェネリック、ブランド、店頭販売ブランド(OTC)、バイオシミラー製品を開発、製造、販売することを専門とするグローバルな非公開製薬会社である。同社は35カ国に2800人の従業員を擁して商業活動を展開、米国、ルーマニア、韓国、台湾で4つの製造・開発拠点を運営している。北米はAlvogenの最大の単一市場であり、その他の主要市場には韓国、ロシア、ルーマニア、ハンガリー、ウクライナ、台湾、日本、中国が含まれる。
Alvogenの詳細については、www.alvogen.com を参照。
▽メディア問い合わせ先
Halldor Kristmannsson
Tel: +354-522-2900
halldor.kristmannsson@alvogen.com
(Logo: リンク )
ソース:Alvogen
御社のプレスリリース・イベント情報を登録するには、ZDNet Japan企業情報センターサービスへのお申し込みをいただく必要がございます。詳しくは以下のページをご覧ください。
 メルカリが「2四半期連続のMAU減少」を恐れない理由--日本事業責任者が語る【インタビュー】
メルカリが「2四半期連続のMAU減少」を恐れない理由--日本事業責任者が語る【インタビュー】
 なぜPayPayは他のスマホ決済を圧倒できたのか--「やり方はADSLの時と同じ」とは
なぜPayPayは他のスマホ決済を圧倒できたのか--「やり方はADSLの時と同じ」とは
 AIが通訳するから英語学習は今後「オワコン」?--スピークバディCEOの見方は
AIが通訳するから英語学習は今後「オワコン」?--スピークバディCEOの見方は
 パラマウントベッド、100人の若手が浮き彫りにした課題からCVCが誕生
パラマウントベッド、100人の若手が浮き彫りにした課題からCVCが誕生
 野村不動産グループが浜松町に本社を「移転する前」に実施した「トライアルオフィス」とは
野村不動産グループが浜松町に本社を「移転する前」に実施した「トライアルオフィス」とは
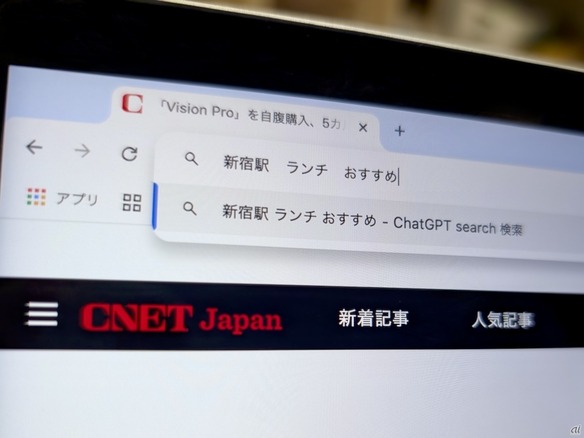 「ChatGPT Search」の衝撃--Chromeの検索窓がデフォルトで「ChatGPT」に
「ChatGPT Search」の衝撃--Chromeの検索窓がデフォルトで「ChatGPT」に
 「S.RIDE」が目指す「タクシーが捕まる世界」--タクシー配車のエスライド、ビジネス向け好調
「S.RIDE」が目指す「タクシーが捕まる世界」--タクシー配車のエスライド、ビジネス向け好調
 物流の現場でデータドリブンな文化を創る--「2024年問題」に向け、大和物流が挑む効率化とは
物流の現場でデータドリブンな文化を創る--「2024年問題」に向け、大和物流が挑む効率化とは
 「ビットコイン」に資産性はあるのか--積立サービスを始めたメルカリ、担当CEOに聞いた
「ビットコイン」に資産性はあるのか--積立サービスを始めたメルカリ、担当CEOに聞いた
 培養肉の課題は多大なコスト--うなぎ開発のForsea Foodsに聞く商品化までの道のり
培養肉の課題は多大なコスト--うなぎ開発のForsea Foodsに聞く商品化までの道のり
 過去の歴史から学ぶ持続可能な事業とは--陽と人と日本郵政グループ、農業と物流の課題解決へ
過去の歴史から学ぶ持続可能な事業とは--陽と人と日本郵政グループ、農業と物流の課題解決へ
 通信品質対策にHAPS、銀行にdポイント--6月就任のNTTドコモ新社長、前田氏に聞く
通信品質対策にHAPS、銀行にdポイント--6月就任のNTTドコモ新社長、前田氏に聞く
 「代理店でもコンサルでもない」I&COが企業の課題を解決する
「代理店でもコンサルでもない」I&COが企業の課題を解決する