◎韓国バイオ企業RNL BIOが骨関節炎治療の幹細胞の第2相をFDAに申請
AsiaNet 52899
共同JBN 0502(2013.5.7)
【ジャーマンタウン(米メリーランド州)2013年5月3日PRN=共同JBN】韓国のバイオ企業RNL BIOはこのほど、骨関節炎(OA)治療のため、RNL-JointStemと呼称されるヒト脂肪由来幹細胞製品による臨床試験を開始するため、米食品医薬品局(FDA)に新薬臨床試験開始届(IND)を提出したと発表した。RNLバイオは、各種の変性、虚血性、その他症状に対する自己細胞治療製品の商品化を専業としている。RNL BIOはFDAの生物学的製剤評価研究センター(CBER)からIND認可を取得することを想定して、米テキサス州シュガーランドで2013年第3四半期中に二重盲検、無作為、陽性対照による第2相臨床試験を開始する計画である。スタンフォード大学のジェイスン・ドラグー博士、インディアナ大学デービッド・アラン・フィッシャー博士が審査役を務め、FDAが現在評価中のプロトコルの見直しを完了した。RNL-JointStemの第1相および第2相臨床試験は既に、韓国食品医薬品安全庁(KFDA)の下で完結している。
RNL BIOのラ・ジェンチャン最高経営責任者(CEO)兼会長は「われわれはRNL-JointStemのINDを提出して喜んでいる。これによって米国でRNL-JointStemの臨床試験に近づける。われわれがこの試験で目指すものは、RNL-JointStemが有効であることを世界的に実証して見せることである。われわれの臨床試験が成功すれば、患者自身の脂肪組織に由来する幹細胞製品を使う骨関節炎の治療でパラダイムシフトにつながるだろう」と語った。RNL-JointStemのこれまでの臨床試験で示された主要な利点として示されたのは、特に骨関節炎治療で現在利用されている多くの侵襲性治療と違い1回の(静脈)注射で症状を管理することである。同CEOは「この苦痛を伴う慢性症状の治療は、それ以上悪化しないよう痛みを和らげることである。われわれはOA患者の軟骨再生、苦痛の緩和、関節機能改善に対するRNL-JointStemの効能を確かめ、しかるべき時期に製品化したいと考えている」と述べた。
臨床試験はヒアルロン酸(HA)を利用して、既存の手順とRNL-JointStemとを比較する。この当初臨床試験を受ける患者集団には、骨関節炎と診断され、担当医が臨床試験候補基準に見合うと判断した患者が含まれる。RNL-JointStemが意図する対象は、現在有効な治療法のない60歳以下の患者である。
▽骨関節炎について
変性性関節炎(DA)は最も一般的な関節炎である。25歳以上の2690万人の米国人が苦痛を伴い、一部関節に臨床的なDAを発症すると推定されており、年齢が上の人の発症率はさらに高くなると考えられている。その臨床所見は関節痛、運動機能障害などで、周辺細胞組織が局部的炎症に冒されることが多い。DAの病因は完全には解明されていないが、負傷、年齢、遺伝子がリスク要因の中に考えられている。
変性性関節炎(DA)は徐々に消耗、活力を失う疾患であり、主として軟骨を冒し、関連する骨の変質を伴う。軟骨は本来の回復・再生能力が制限されている。
▽今回の臨床試験を通じて
変性性関節炎(DA)の症例と高齢者人口が増加しているため、効果的な治療選択肢、最新の軟骨修復方針が必要になっている。この症状に対する治療法として有効な製品市場は非常に大きいと推定されている。
▽新薬臨床試験開始届(IND)について
新薬臨床試験開始届(IND)は、米国における臨床試験実施許認可の手続きである。INDは、米国での臨床試験の実施を意図するものであることが必要である。INDは治験薬の質、製造、管理および臨床前研究データ、臨床上の利用の意志に関連する情報を含む。意図する研究であり得るリスクとベネフィットに関連する全体的なリスク・ベネフィット評価および臨床前データのクリティカル分析は、INDの一部として提出するよう求められている。
▽第2相臨床試験について
生物学、自分自身の細胞由来幹細胞を含む生物製剤を使用する臨床的措置の研究は、FDAの生物学的製剤評価研究センター(CBER)によって厳格に管理される。臨床試験のフェーズ(相)シリーズは、INDがCBERと地域の治験審査委員会 (IRB)で受理されることが決まった後、FDAの承認が必要となる。第1相が重視する点は安全性であり、第2相は有効性(効能)を強調する。第2相臨床試験は研究の有効性(処方量によってどれほど生物学的に有効かどうか)についてより明快に説明されることを目指している。
▽RNL BIOについて
RNL BIOは韓国のバイオテクノロジー企業であり、成人由来の幹細胞テクノロジーの研究と開発に注力している。RNLは韓国の韓国食品医薬品安全庁(KFDA)の下で、脊椎損傷に対する(ある幹細胞の)第1相試験を完了し、骨関節炎に対する(ある幹細胞の)第2相試験も完了、さらにバージャー病の臨床試験の完了間近である。
このプレスリリースに触れられていない詳しい情報は
リンクを参照。
ソース:RNL BIO
▽問い合わせ先
Jin Hong
+82-10-6213-0686
hongjh@rnl.co.kr
御社のプレスリリース・イベント情報を登録するには、ZDNet Japan企業情報センターサービスへのお申し込みをいただく必要がございます。詳しくは以下のページをご覧ください。
 メルカリが「2四半期連続のMAU減少」を恐れない理由--日本事業責任者が語る【インタビュー】
メルカリが「2四半期連続のMAU減少」を恐れない理由--日本事業責任者が語る【インタビュー】
 なぜPayPayは他のスマホ決済を圧倒できたのか--「やり方はADSLの時と同じ」とは
なぜPayPayは他のスマホ決済を圧倒できたのか--「やり方はADSLの時と同じ」とは
 AIが通訳するから英語学習は今後「オワコン」?--スピークバディCEOの見方は
AIが通訳するから英語学習は今後「オワコン」?--スピークバディCEOの見方は
 パラマウントベッド、100人の若手が浮き彫りにした課題からCVCが誕生
パラマウントベッド、100人の若手が浮き彫りにした課題からCVCが誕生
 野村不動産グループが浜松町に本社を「移転する前」に実施した「トライアルオフィス」とは
野村不動産グループが浜松町に本社を「移転する前」に実施した「トライアルオフィス」とは
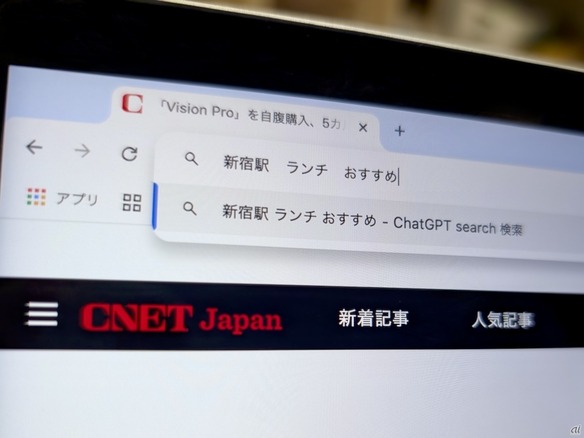 「ChatGPT Search」の衝撃--Chromeの検索窓がデフォルトで「ChatGPT」に
「ChatGPT Search」の衝撃--Chromeの検索窓がデフォルトで「ChatGPT」に
 「S.RIDE」が目指す「タクシーが捕まる世界」--タクシー配車のエスライド、ビジネス向け好調
「S.RIDE」が目指す「タクシーが捕まる世界」--タクシー配車のエスライド、ビジネス向け好調
 物流の現場でデータドリブンな文化を創る--「2024年問題」に向け、大和物流が挑む効率化とは
物流の現場でデータドリブンな文化を創る--「2024年問題」に向け、大和物流が挑む効率化とは
 「ビットコイン」に資産性はあるのか--積立サービスを始めたメルカリ、担当CEOに聞いた
「ビットコイン」に資産性はあるのか--積立サービスを始めたメルカリ、担当CEOに聞いた
 培養肉の課題は多大なコスト--うなぎ開発のForsea Foodsに聞く商品化までの道のり
培養肉の課題は多大なコスト--うなぎ開発のForsea Foodsに聞く商品化までの道のり
 過去の歴史から学ぶ持続可能な事業とは--陽と人と日本郵政グループ、農業と物流の課題解決へ
過去の歴史から学ぶ持続可能な事業とは--陽と人と日本郵政グループ、農業と物流の課題解決へ
 通信品質対策にHAPS、銀行にdポイント--6月就任のNTTドコモ新社長、前田氏に聞く
通信品質対策にHAPS、銀行にdポイント--6月就任のNTTドコモ新社長、前田氏に聞く
 「代理店でもコンサルでもない」I&COが企業の課題を解決する
「代理店でもコンサルでもない」I&COが企業の課題を解決する